
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
BABIO برای کیت انتقال ویروس خود (غیرفعالکننده) مجوز FDA 510(k) را تضمین میکند.
BABIO برای کیت انتقال ویروس خود (غیرفعالکننده) مجوز FDA 510(k) را تضمین میکند.
جینان، چین – اکتبر 2025 – شرکت بیوتکنولوژی جینان بابیو (BABIO)با افتخار اعلام می کند کهکیت انتقال ویروس Babio® (غیرفعالکننده)رسما دریافت کرده استترخیص کالا از گمرک FDA 510 (k) (K250205). این گواهی نقطه عطف مهمی برای BABIO است و تعهد آن را به کیفیت، ایمنی و نوآوری جهانی در تشخیص بالینی و سیستمهای حمل و نقل میکروبیولوژیکی تأیید میکند.
مجوز 510 (k) FDA به کیت انتقال ویروس Babio® اجازه می دهدبه طور قابل ملاحظه ای معادلبه دستگاه هایی که به طور قانونی در ایالات متحده به بازار عرضه می شوند، و مطابقت آن با استانداردهای نظارتی ایالات متحده برای دستگاه های پزشکی را تأیید می کند. این دستاورد توانایی های R&D قوی و برتری تولید BABIO را نشان می دهد و رقابت جهانی آن را بیشتر تقویت می کند.بازار حمل و نقل ویروس و جمع آوری نمونه.
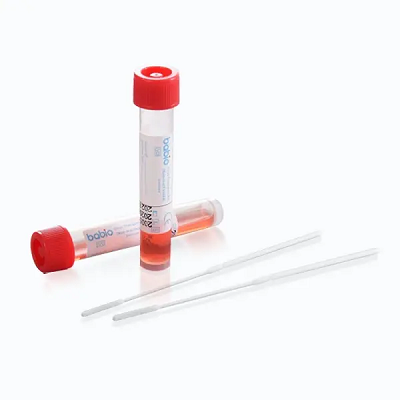
اینکیت انتقال ویروس Babio® (غیرفعالکننده)برای جمع آوری و حمل و نقل ایمن نمونه های بالینی حاوی ویروس طراحی شده است. این یکپارچگی نمونه را برای تست های پایین دستی مانندRT-PCR, فرهنگ ویروسی، وتشخیص مولکولی، آن را برای بیمارستان ها، آزمایشگاه ها و موسسات بهداشت عمومی در سراسر جهان مناسب می کند.

بابیو، بهتولید کننده پیشرو چینیمعرفهای تشخیصی، رسانههای انتقال و محیطهای کشت، همچنان به گسترش حضور خود در این کشور ادامه میدهداروپا، ایالات متحده، آفریقا و آسیای جنوب شرقی، ارائه راه حل های قابل اعتماد که مطابق با استانداردهای بین المللی است.
برای کسب اطلاعات بیشتر در مورد محصولات تایید شده BABIO و نوآوری های تشخیصی، لطفاً از: https://www.babiocorp.com
#BABIO #FDA510k #VirusTransportKit #دستگاههای پزشکی #تشخیص #BiotechChina #GlobalHealthcare #ClinicalDiagnostics #Microbiology


